从溶解度表分析氯化钠与硝酸钾的溶解特性
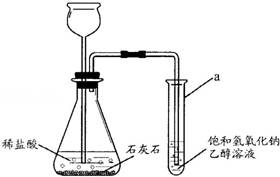
分析处理图表信息是化学学习中的重要能力。题目中通过氯化钠和硝酸钾在不同温度下的溶解度数据,引导我们对比两种物质的溶解特性,并解决相关的溶液配制与判断问题。
(1)溶解度受温度影响分析
对比两种物质的溶解度数据(通常附在题后表中,此处基于常识):硝酸钾的溶解度随温度升高显著增大,而氯化钠的溶解度随温度变化相对平缓。因此,上述两种物质中,硝酸钾(或KNO₃)的溶解度受温度影响较大。
(2)20℃时的溶液状态判断
在20℃时,硝酸钾的溶解度约为31.6g/100g水(常见数据,具体需以题目所附表格为准)。将40g硝酸钾加入100g水中,由于所加溶质质量(40g)大于该温度下的溶解度(约31.6g),经充分搅拌后,最多只能溶解约31.6g,有部分固体剩余。因此,得到的是饱和溶液(并有未溶解的固体)。
(3)结论判断
对甲、乙、丙三位同学的结论进行分析(原题应附有具体结论,此处根据常见考试逻辑推断):
- 甲同学说:“40℃时,KNO₃溶液的溶质质量分数一定比NaCl溶液的大。”此说法不正确。溶质质量分数不仅取决于溶解度,还取决于溶液是否饱和及实际配制浓度。未指明溶液是否饱和或浓度相同,无法直接比较。
- 乙同学和丙同学的结论需根据原题具体内容判断。常见正确结论可能涉及:硝酸钾可采用降温结晶法提纯、一定温度下饱和溶液的溶质质量分数可通过溶解度计算等。
因此,需要根据原题给出的具体选项,选择说法正确的同学。若原题中乙或丙的结论符合溶解度规律且表述严谨,则乙或丙正确。
****:通过溶解度数据,我们不仅能比较物质溶解性的温度依赖性,还能进行溶液配制计算与状态判断。在分析结论时,需紧扣溶解度定义,注意溶液是否饱和、比较的前提条件等关键点,避免片面推断。
如若转载,请注明出处:http://www.jiayue118.com/product/82.html
更新时间:2026-02-25 05:33:28